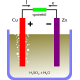
Galvanický článok
Galvanické články využívajú chemickú reakciu, pri ktorej sa uvoľňuje energia vo forme elektrického poľa. Pri chemickej reakcii má molekula novovzniknutej zlúčeniny menšiu energiu než súčet energií častí, z ktorých vznikla. Galvanických článkov existuje mnoho druhov. Niektoré sa dajú opakovane nabíjať, pretože elektrochemické deje, ktoré v nich prebiehajú, sú vratné. Galvanické články patria medzi primárne články – môžeme z nich elektrický prúd odoberať bez toho, že by sme im ho predtým „dodali“.
Najjednoduchší galvanický článok sa skladá z elektrolytu a dvoch elektród. Ako elektrolyt sa používa kyselina sírová. Kladná elektróda je z medi a záporná zo zinku. Po zriedení kyseliny sírovej vodou molekuly vody uvoľňujú pevnú väzbu molekúl kyseliny, ktorá sa rozštiepi na kladné a záporné ióny. Medzi nábojmi je ale rovnováha a elektrolyt zostáva elektricky neutrálny. Po ponorení zinkovej elektródy do elektrolytu sa začne zinok rozpúšťať a jeho katióny nabíjajú elektrolyt kladne. Zinková elektróda sa nabíja záporne a medzi kladnou a zápornou elektródou sa objaví napätie 1,05 V. Ak na svorky galvanického článku pripojíme spotrebič, poruší sa rovnovážny stav, elektróny sa cez spotrebič odvádzajú zo zinkovej elektródy na elektródu medenú, a vzniká tak elektrický prúd.
Prvé galvanické články boli mokré s tekutým elektrolytom. Dnes sa najviac používajú suché články, ktoré majú medzi elektródami pórovitú hmotu nasýtenú elektrolytom.
Typy galvanických článkov: suché Leclancheove články, alkalické a ortuťové články,
Tvar: valcový, plochý a hranatý,
Použitie: vreckové svietidlá, rozhlasové prístroje, prenosné vysielače a prijímače, ďalšie drobné prístroje denného použitia.